Diabetes Typ 2
Inhaltsverzeichnis
Basis-Info: Zuckerstoffwechsel und Insulin
Alle Zellen des Körpers brauchen Zucker, um richtig zu funktionieren. Zucker liefert den Muskeln und Organen Energie für ihre Arbeit. Bis der Zucker aus der Nahrung dort ankommt, wo er gebraucht wird – im Inneren der Zellen –, laufen verschiedene Vorgänge ab:
Zucker gelangt mit der Nahrung in den Darm. Dort wird er aus der Nahrung gefiltert, aufgespalten und ins Blut aufgenommen. Der Blutzuckerspiegel steigt an. Über den Blutkreislauf wird der Zucker zu den Zellen verteilt. Damit die Zellen den Zucker verwerten und in Energie umwandeln können, muss er in die Zellen hineingelangen. Dafür ist das Hormon Insulin zuständig: Es sorgt dafür, dass der Zucker aus dem Blut in die Zellen aufgenommen wird. In der Folge nimmt der Zuckergehalt im Blut ab.
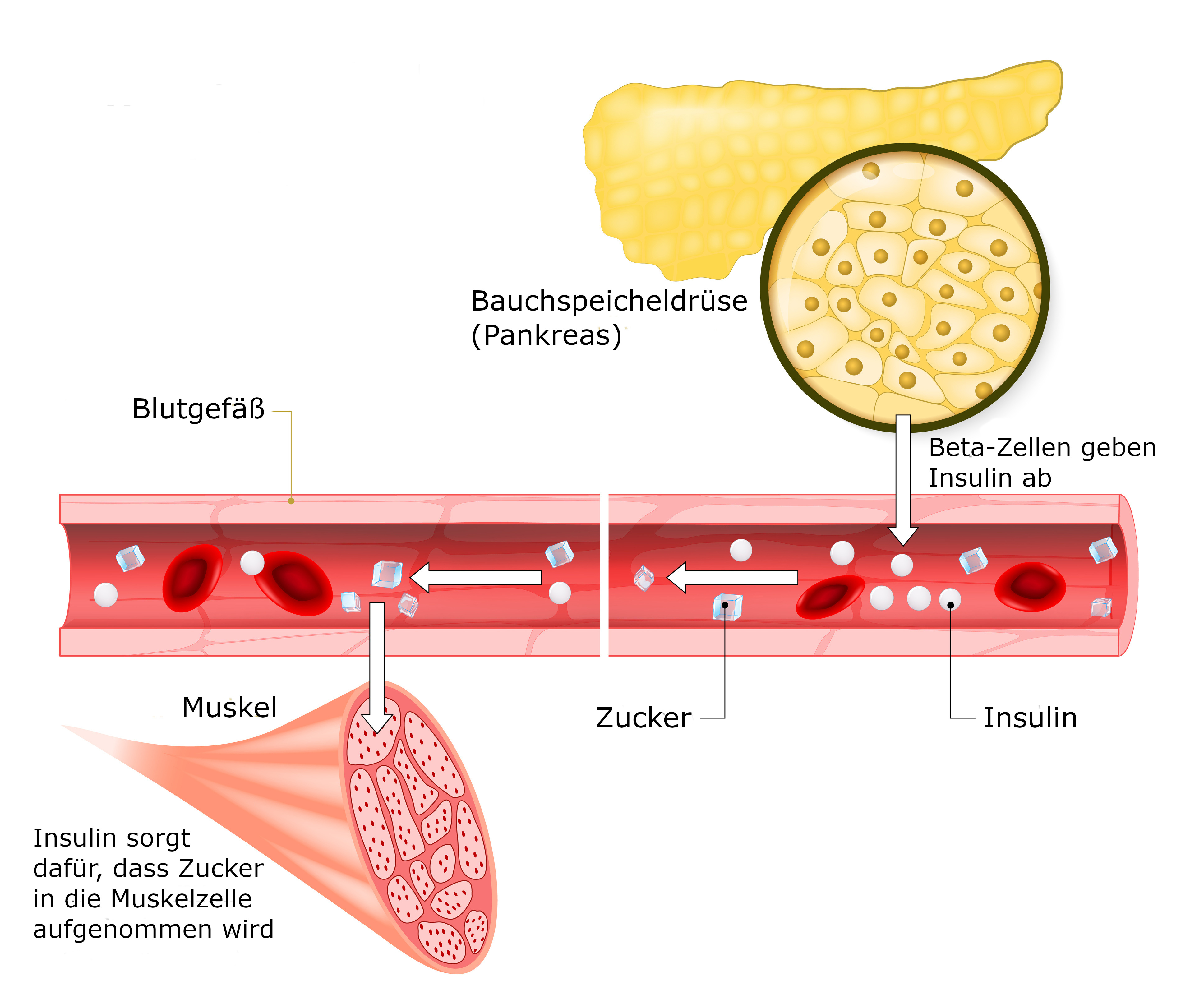
Das Insulin wird in den sogenannten Betazellen der Bauchspeicheldrüse produziert. Die Bauchspeicheldrüse misst dauernd, wie hoch der Blutzuckerspiegel ist: Ist er hoch, schüttet sie Insulin aus, um ihn zu senken.
Wie entsteht Diabetes Typ 2?
Typ-2-Diabetes entsteht über einen langen Zeitraum. Durch verschiedene Faktoren – z.B. einer ungesunden Lebensweise - kommt es zu einer Unempfindlichkeit gegenüber Insulin. Das bedeutet: Es ist zwar genug Insulin vorhanden, die Zellen reagieren aber nicht entsprechend darauf. Sie nehmen den Zucker aus dem Blut weniger gut auf. Fachleute sprechen von einer Insulinresistenz.
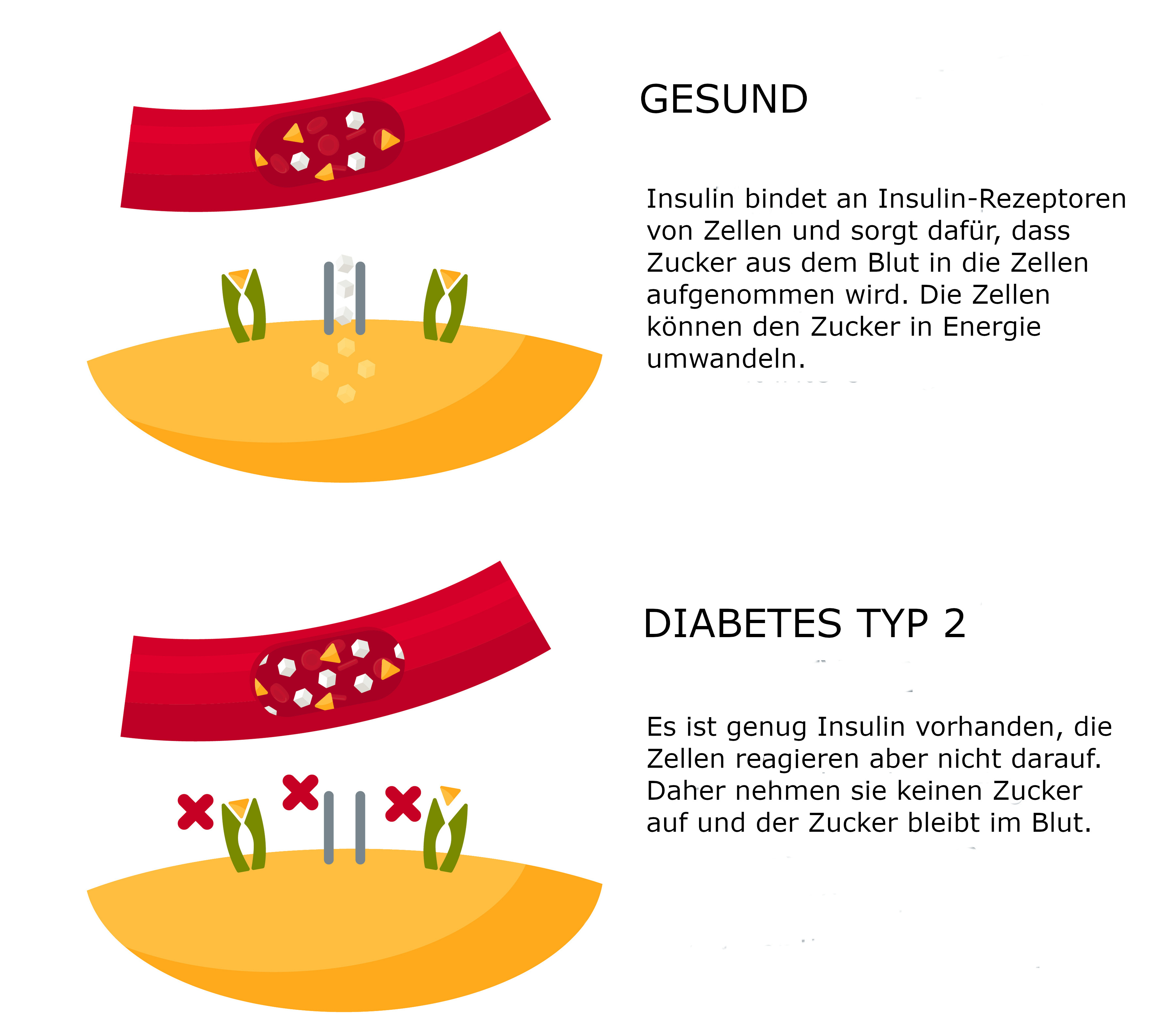
Die Bauchspeicheldrüse muss immer mehr Insulin produzieren, um den Blutzucker trotzdem zu senken. Irgendwann kann sie das bei entsprechender genetischer Veranlagung nicht mehr gewährleisten: Die Betazellen der Bauchspeicheldrüse erschöpfen, und die Insulinproduktion nimmt ab. Es entsteht ein zunehmender Insulinmangel, und der Blutzuckerwert steigt an. Ein erhöhter Blutzuckerwert wird auch als Hyperglykämie bezeichnet. Ein dauerhaft erhöhter Blutzuckerwert führt letztlich zur Diagnose Diabetes.
Hinweis
Bei Personen mit Typ-2-Diabetes produziert der Körper zunächst genug Insulin. Es kann aber nicht mehr richtig wirken. Wenn die Erkrankung weiter fortschreitet, nimmt auch die Insulinproduktion immer weiter ab.
Welche Risikofaktoren gibt es?
Verschiedene Faktoren erhöhen das Risiko für eine Insulinresistenz bzw. für Typ-2-Diabetes. Dazu zählen:
- höheres Alter
- Übergewicht
- Bewegungsmangel
- fettreiche und ballaststoffarme Ernährung
- erhöhte Blutfettwerte
- erhöhter Blutdruck
- Typ-2-Diabetes in der Familie
- Rauchen
- bestimmte Medikamente
- Schwangerschaftsdiabetes
Meistens liegt eine Kombination mehrerer Risikofaktoren vor. Eine große Rolle bei der Entstehung einer Insulinresistenz scheint Übergewicht zu spielen. Eine Insulinresistenz besteht meist schon Jahre, bevor die Diagnose Prädiabetes oder Diabetes gestellt wird.
Hinweis
Die Kombination aus Bluthochdruck, erhöhten Blutfettwerten und erhöhten Blutzuckerwerten wird auch als metabolisches Syndrom bezeichnet.
Was ist Prädiabetes?
Prädiabetes ist eine Vorstufe von Typ-2-Diabetes. Das bedeutet: Es liegt eine Insulinresistenz vor, und der Zuckerstoffwechsel ist bereits gestört. Die Blutzuckerwerte sind höher als bei gesunden Personen, aber noch nicht so hoch wie bei Personen mit Typ-2-Diabetes. Fachleute sprechen auch von einer gestörten Glukosetoleranz.
Personen mit Prädiabetes haben ein sehr hohes Risiko, innerhalb der nächsten Jahre an Diabetes zu erkranken. Auch das Risiko für andere Erkrankungen ist erhöht, z.B. für Herz-Kreislauf-Erkrankungen oder einen Schlaganfall.
Personen mit Prädiabetes können die Entstehung eines Typ-2-Diabetes noch verhindern oder zumindest verzögern. Wenn rechtzeitig gegengesteuert wird, z.B. durch eine Gewichtsabnahme und eine gesunde Lebensweise, können die Blutzuckerwerte wieder in den Normalbereich zurückkehren.
Welche Symptome können auftreten?
Typ-2-Diabetes entwickelt sich schleichend und macht oft lange Zeit keine Beschwerden. Bei dauerhaft erhöhten Blutzuckerwerten können unterschiedliche Symptome auftreten, zum Beispiel:
- starker Durst,
- häufiges Urinieren, auch nachts,
- Müdigkeit, Antriebsschwäche,
- Übelkeit,
- Schwindel,
- unscharfes Sehen,
- häufige Infekte,
- trockene Haut, häufige Hautinfektionen,
- schlechte Wundheilung.
Wenn die Blutzuckerwerte über längere Zeit sehr hoch sind, kann eine schwere Stoffwechselentgleisung entstehen. Sie kann zu Bewusstseinsstörungen, Bewusstlosigkeit bis hin zum Koma führen.
Wie wird die Diagnose gestellt?
Die Diagnose Diabetes wird durch Messung des Blutzuckerwertes gestellt. Dafür entnimmt die Ärztin oder der Arzt eine Blutprobe aus der Vene. Der Blutzuckerwert wird anschließend im Labor bestimmt. Für eine sichere Diagnose sind meist mehrere Untersuchungen an verschiedenen Tagen erforderlich.
Mehr zum Thema: Diabetes: Diagnose
| kein Diabetes | Prädiabetes | Diabetes | |
| Nüchternblutzuckerwert | unter 100 mg/dl | 100 bis 125 mg/dl | 126 mg/dl oder mehr |
| HbA1c | unter 5,7 % | 5,7 bis 6,4 % | 6,5 % oder mehr |
| 2-Stunden-Wert des oGTT | unter 140 mg/dl | 140 bis 199 mg/dl | 200 mg/dl oder mehr |
Wie erfolgt die Behandlung von Diabetes Typ 2?
Die Behandlung von Typ-2-Diabetes besteht aus mehreren Bausteinen:
- Die behandelnde Ärztin oder der behandelnde Arzt vereinbart gemeinsam mit der Patientin oder dem Patienten individuelle Ziele, die mit der Therapie erreicht werden sollen.
- Die Basis der Therapie bildet eine Veränderung der Lebensgewohnheiten. Dazu gehört z.B. eine gesunde Ernährung, ausreichend Bewegung und Verzicht aufs Rauchen.
- Unter Umständen ist zusätzlich auch eine medikamentöse Therapie notwendig.
Das Ziel aller therapeutischen Maßnahmen ist es, den Blutzuckerwert langfristig zu senken. Damit soll auch das Risiko für schwere Folgeerkrankungen abnehmen.
Individuelle Therapieziele vereinbaren
Zu Beginn der Therapie werden individuelle Ziele vereinbart, die für die Betroffene oder den Betroffenen realistisch umsetzbar sind. In erster Linie soll der Blutzuckerwert gesenkt werden: Es werden Zielwerte für den Nüchternblutzucker und für den Zuckerwert nach dem Essen festgelegt. Die Patientin oder der Patient kann diese regelmäßig selbst kontrollieren. Auch für den HbA1c-Wert wird ein Zielbereich festgelegt und in regelmäßigen Abständen mittels Blutuntersuchung kontrolliert.
Darüber hinaus werden weitere Ziele vereinbart, z.B.:
- wie hoch die Blutfettwerte höchstens sein sollten,
- wie hoch der Blutdruck höchstens sein sollte,
- welches Körpergewicht angestrebt werden sollte,
- mit dem Rauchen aufzuhören.
Die Ziele werden individuell auf die Patientin oder den Patienten abgestimmt. Sie sind unter anderem abhängig vom Alter, von der Lebenssituation, von eventuellen Begleiterkrankungen und vom allgemeinen Gesundheitszustand.
Gesunder Lebensstil als Basistherapie
In erster Linie wird versucht, die festgelegten Ziele mit einem gesunden Lebensstil zu erreichen. Dazu gehört z.B. regelmäßige Bewegung und eine gesunde, auf Diabetes abgestimmte Ernährung. Betroffene können mit diesen Maßnahmen selbst viel dazu beitragen, den Stoffwechsel positiv zu beeinflussen.
Mehr zum Thema: Diabetes: Lebensstil
Behandlung mit blutzuckersenkenden Medikamenten
Wenn die Zielwerte durch eine Lebensstiländerung alleine nicht erreicht werden können, verordnet die Ärztin oder der Arzt zusätzlich eine medikamentöse Behandlung.
Es gibt verschiedene Medikamente, die den Blutzucker senken. Wenn sie in Form von Tabletten geschluckt werden, werden sie als orale Antidiabetika bezeichnet. Dazu zählen:
- Metformin: Personen mit Typ-2-Diabetes, die eine medikamentöse Behandlung brauchen, erhalten meistens zuerst Metformin. Metformin wirkt auf verschiedene Weise. Unter anderem steigert es die Insulinempfindlichkeit der Zellen. Dadurch kann das körpereigene Insulin besser wirken, und der Blutzuckerwert nimmt ab.
- Sulfonylharnstoffe: Dazu zählen die Substanzen Gliclazid, Glimepirid, Gliquidon. Sie bewirken, dass die Bauchspeicheldrüse mehr Insulin freisetzt. Sulfonylharnstoffe werden oft zusätzlich zu Metformin verordnet, wenn der Blutzucker weiterhin zu hoch ist. Allerdings können sie auch zu Unterzuckerungen - sogenannten Hypoglykämien - führen.
- DPP-4-Hemmer oder Gliptine: Dazu zählen z.B. die Substanzen Sitagliptin, Saxagliptin, Vildagliptin, Linagliptin. Sie können ebenfalls zusätzlich zu Metformin verordnet werden, wenn dessen Wirkung alleine nicht ausreicht. Gliptine bewirken, dass ein bestimmtes Darmhormon langsamer abgebaut wird, das die Ausschüttung von Insulin fördert. Dadurch senken sie den Blutzuckerspiegel.
- Gliflozine oder SGLT-2-Hemmer: Dazu zählen die Substanzen Dapgliflozin, Empagliflozin, Canagliflozin und Ertugliflozin. Sie senken den Blutzucker, indem sie bewirken, dass mehr Zucker mit dem Harn ausgeschieden wird. Gliflozine können zusätzlich zu Metformin verordnet werden. Zudem haben sie günstige Eigenschaft hinsichtlich einer möglichen Herzschwäche oder Nierenfunktionseinschränkung.
- Weitere orale Antidiabetika: Es gibt weitere Medikamente, die den Blutzucker senken können. Dazu zählen unter anderem Alpha-Glucosidase-Inhibitoren, z.B. Acarbose, oder Glinide, z.B. Repaglinid, oder Glitazone, z.B. Pioglitazon. Sie werden heute selten bzw. nur in speziellen Situationen eingesetzt.
Es gibt auch blutzuckersenkende Wirkstoffe, die nicht als Tablette eingenommen, sondern unter die Haut gespritzt werden. Sie gehören zur Gruppe der GLP-1-Analoga oder Inkretinmimetika. Es gibt die Substanzen Exenatid, Liraglutid, Semaglutid, Lixisenatid und Dulaglutid. GLP-1-Analoga wirken ähnlich, aber etwas stärker als Gliptine. Sie bewirken unter anderem, dass die Bauchspeicheldrüse mehr Insulin freisetzt. GLP-1-Analoga können darüber hinaus dabei helfen, Gewicht zu reduzieren, weil sie ein Sättigungsgefühl auslösen. Zudem haben sie günstige Effekte hinsichtlich atherosklerotischer Folgeerkrankungen wie Herzinfarkt und Schlaganfall.
Hinweis
Die genannten Medikamente senken nicht nur den Blutzucker, sie sollen vor allem auch schwere Folgeerkrankungen von Diabetes verhindern.
Die einzelnen Wirkstoffe haben verschiedene zusätzliche Effekte, z.B. auf das Körpergewicht, auf den Blutdruck oder auf die Blutfettwerte. Zudem haben sie jeweils andere Nebenwirkungen und gehen mit einem unterschiedlich hohen Risiko für Unterzuckerungen einher. Nicht jeder Wirkstoff ist für jede Person mit Diabetes geeignet. Welche Behandlung individuell infrage kommt, hängt von verschiedenen Faktoren ab, z.B. vom Alter oder ob ein erhöhtes Risiko für Herz-Kreislauf-Erkrankungen oder für Nierenerkrankungen besteht. Die Ärztin oder der Arzt berücksichtigt diese Aspekte bei der Auswahl der individuellen Therapie.
Insulintherapie
Bei Typ-2-Diabetes produziert die Bauchspeicheldrüse zunächst meist genug Insulin. Wenn die Erkrankung weiter fortschreitet, nimmt die Insulinproduktion jedoch ab. Dann müssen auch Personen mit Typ-2-Diabetes Insulin zuführen.
Mehr zum Thema: Diabetes: Insulintherapie
Bei der Behandlung von Diabetes sind regelmäßige Arzttermine und Kontrolluntersuchungen notwendig. Eine wichtige Hilfe für die Dokumentation und Planung ist der Diabetes-Pass. Darin trägt die Ärztin oder der Arzt z.B. Untersuchungsergebnisse, Behandlungsschritte und Termine für Kontrollen ein. Dadurch wird der Krankheitsverlauf dokumentiert. Personen mit Diabetes erhalten den Pass bei der behandelnden Ärztin oder dem behandelnden Arzt oder der Krankenkasse.
Kontrolluntersuchungen
Regelmäßige Kontrolluntersuchungen sind wichtig, damit die behandelnde Ärztin oder der behandelnde Arzt prüfen kann, ob die vereinbarten Therapieziele erreicht werden. Falls nicht, muss die Behandlung unter Umständen angepasst werden.
Die Kontrolluntersuchungen dienen auch dazu, eventuelle Folgeerkrankungen rechtzeitig zu erkennen. Zu den regelmäßigen Untersuchungen gehören unter anderem Untersuchungen des Blutbildes, des Augenhintergrundes, des Harnes oder der Füße.
Hinweis
Für den Erfolg der Behandlung sind die Mitarbeit und die Motivation der Patientinnen und Patienten von entscheidender Bedeutung.
Welche Komplikationen können bei Diabetes auftreten?
Die häufigsten akuten Komplikationen bei Diabetes sind Überzuckerungen oder Unterzuckerungen. Sie sind teils Folge der Erkrankung selbst, teils Folge der Behandlung. Sie können im Extremfall zu lebensbedrohlichen Notfallsituationen führen.
Mehr zum Thema: Diabetes: Überzuckerung und Unterzuckerung
Welche Folgeerkrankungen können bei Diabetes auftreten?
Diabetes kann langfristig schwerwiegende gesundheitliche Probleme nach sich ziehen. Ein dauerhaft erhöhter Blutzuckerspiegel führt z.B. zu einer Schädigung der kleinsten Blutgefäße und der Nerven. In der Folge können Erkrankungen der Nieren, der Augen oder des Herzens auftreten.
Mehr zum Thema: Diabetes: Folgeerkrankungen
Was ist eine Patientenschulung?
Patientenschulungen haben das Ziel, Personen mit chronischen Erkrankungen zu unterstützen. Der Alltag ändert sich nach einer Diabetesdiagnose. Betroffene müssen lernen, ihren Lebensstil anzupassen. Sie müssen selbstständig ihren Blutzucker kontrollieren und die Medikamente entsprechend einnehmen. Es ist wichtig, dass Personen mit Diabetes über ihre Erkrankung gut informiert sind. Der Besuch spezieller Schulungen hilft dabei, das nötige Wissen zu erlangen und den Alltag zu meistern.
In Patientenschulungen erfahren die Teilnehmerinnen und Teilnehmer unter anderem:
- wie sie den Blutzucker selbst messen und kontrollieren können,
- warum eine gesunde Ernährung so wichtig ist und wie man sie umsetzen kann,
- warum Bewegung so wichtig ist und wie man sie umsetzen kann,
- wie die Medikamente wirken und wie sie eingenommen werden müssen,
- wie Insulin verabreicht wird,
- was bei akuten Komplikationen, z.B. Unterzuckerung, zu tun ist.
Patientenschulungen umfassen mehrere Termine und haben das Ziel, die Betroffenen schrittweise zu mehr Eigenverantwortung zu führen. Sie werden von speziell ausgebildeten Ärztinnen und Ärzten oder Diabetes-Beraterinnen und -Beratern durchgeführt.
Disease-Management-Programm - Therapie Aktiv
Patientenschulungen sind oft Bestandteil sogenannter Disease-Management-Programme, kurz DMP. Darunter versteht man qualitätsgesicherte Behandlungsprogramme, die eine optimale Betreuung jeder Patientin bzw. jedes Patienten sicherstellen sollen. Die Programme umfassen neben Schulungen unter anderem individuell zugeschnittene Therapiekonzepte.
In Österreich gibt es für Personen mit Diabetes das Disease-Management-Programm „Therapie Aktiv“ der Sozialversicherung. Ziel des Programmes ist es, akute Gesundheitsprobleme der Betroffenen zu vermeiden, Spätfolgen einzudämmen und ihre Lebensqualität zu verbessern. Das Programm sieht regelmäßige Arztbesuche vor, bei denen der Krankheitsverlauf kontrolliert und dokumentiert wird. Eine Ärztin bzw. ein Arzt des Therapie-Aktiv-Programms mit spezieller Ausbildung begleitet Personen mit Diabetes und koordiniert die Untersuchungen sowie weitere Behandlungen in spezialisierten Einrichtungen. Ein wichtiger Teil sind zudem die Schulungen der Betroffenen, in denen sie lernen, mit ihrer Erkrankung richtig umzugehen.
Die Teilnahme an Therapie Aktiv ist kostenlos. Weitere Informationen finden Sie auf der Homepage Therapie Aktiv.
Video: Diabetes - einfach erklärt
Ein Erklär-Video für alle, die erfahren möchten, was Diabetes ist und wie Diabetes entsteht.
Wohin kann ich mich wenden?
Für die Diagnose und die Behandlung von Diabetes können Sie sich an folgende Stellen wenden:
- Ärztin bzw. Arzt für Allgemeinmedizin
- Fachärztin bzw. Facharzt für Innere Medizin mit dem Zusatzfach Endokrinologie und Stoffwechsel
- Diabetes-Ambulanzen (Österreichische Diabetesgesellschaft)
- „Therapie Aktiv“-Ärztinnen und -Ärzte
Die behandelnde Ärztin oder der behandelnde Arzt wird oft von Expertinnen und Experten aus anderen Gesundheitsberufen unterstützt, z.B. Diätologinnen und Diätologen oder Psychologinnen und Psychologen. Bei Bedarf werden auch andere Fachärztinnen und Fachärzte hinzugezogen, z.B. für Nervenerkrankungen (Neurologie), Nierenerkrankungen (Nephrologie), Herzerkrankungen (Kardiologie) oder Gefäßchirurgie.
Wie erfolgt die Abdeckung der Kosten?
Die e-card ist Ihr persönlicher Schlüssel zu den Leistungen der gesetzlichen Krankenversicherung. Alle notwendigen und zweckmäßigen Diagnose- und Therapiemaßnahmen werden von Ihrem zuständigen Sozialversicherungsträger übernommen. Bei bestimmten Leistungen kann ein Selbstbehalt oder Kostenbeitrag anfallen. Detaillierte Informationen erhalten Sie bei Ihrem Sozialversicherungsträger. Weitere Informationen finden Sie außerdem unter:
- Recht auf Behandlung
- Arztbesuch: Kosten und Selbstbehalte
- Was kostet der Spitalsaufenthalt
- Rezeptgebühr: So werden Medikamentenkosten abgedeckt
- Reha & Kur
- Heilbehelfe & Hilfsmittel
- Gesundheitsberufe A-Z
sowie über den Online-Ratgeber Kostenerstattung der Sozialversicherung.
Die verwendete Literatur finden Sie im Quellenverzeichnis.
Letzte Aktualisierung: 12. Januar 2023
Erstellt durch: Redaktion Gesundheitsportal
Expertenprüfung durch: Prim. Univ.Prof. Dr. Bernhard Ludvik, Facharzt für Innere Medizin, Zusatzfach Innere Medizin (Endokrinologie u. Stoffwechselerkr.)

